AAIC 2020

Imaging Biomarkers and Alzheimer’s Prevention
한림대병원 김여진
-
Imaging biomarker
알츠하이머병의 진단은 amyloid, tau, neurodegeneration을 측정하여 진단을 한다. 알츠하이머병은 beta amyloid 가 tau accumulation을 유발하고 이 것이 brain atrophy를 가속화하여 cognitive decline을 초래해 dementia 증상을 일으킨다. 알츠하이머병의 imaging biomarker 중에서 tau accumulation과 neurodegeneration은 알츠하이머병에 특이적인 마커는 아니나 증상과의 연관성이 높고 amyloid beta accumulation은 가장 먼저 일어나기는 하지만 알츠하이머병 증상과 연관성은 낮다.
-
임상적인 진단과 biomarker 기반 진단의 불일치
-
알츠하이머병으로 임상 진단을 받은 사람 중 아밀로이드 배타 음성인 사람 또는 아밀로이드 베타 양성이나 타우 축적이 적은 사람
- APOE e4 non-carrier
- 80세 이상 고령
- 남성
- Less cognitive decline
- More cerebrovascular and other pathology
-
알츠하이머병으로 임상 진단을 받은 사람 중 아밀로이드 베타 양성인 사람 또는 아밀로이드 베타 양성이면서 타우 축적이 높은 사람 ➔ amyloid beta pathway
- APOE e4 carrier
- 75세 이하의 젊은 연령
- 여성
- More cognitive decline
- More “pure” AB/tau pathology
-
인지기능 정상인 중 아밀로이드 양성으로 전환되지 않은 사람
- APOE e4 non-carrier
- 남성
- Less cognitive decline
- More cerebrovascular and other pathology
-
인지기능 정상인 중 아밀로이드 양성으로 전환된 사람 ➔ amyloid beta pathway
- APOE e4 carrier
- 여성
- More cognitive decline (5년 뒤 기억력 저하가 더 심함)
- More “pure” AB/tau pathology (5년 뒤 tau PET uptake 증가)
-
-
적합한 amyloid, tau targeted therapy
- 대상군: amyloid beta pathway를 따르는 사람
- 적합한 시기
Primary prevention intervention: 아밀로이드 베타 축적이 시작하여 축적의 속도가 느려질 때까지인 7-10년
Secondary prevention intervention: 아밀로이드 베타 축적의 속도가 느려진 후 경도인지장애 증상을 보일 때까지 시기인 약 10년 - APOE e4 carrier: APOE e4 non-carrier 보다 15-19년 빨리 amyloid 양성 threshold에 도달
-
amyloid beta pathway를 따르지 않는 사람들의 예방 및 치료
Amyloid beta pathway를 따르지 않는 사람들은 cerebrovascular pathology가 더 많다. 혈관성 위험요인과 아밀로이드 베타가 synergistic effect를 보인 연구 결과도 있고, LDL cholesterol 이 높을수록 amyloid beta accumulation 이 증가한 연구 결과도 있다.
FINGER study 나 SPRINT-MIND trial에서 vascular risk factor를 줄이는 intervention을 시행하여 인지저하 예방에 도움이 됨을 보였다. 하지만 intervention이 뇌내 알츠하이머병의 병리소견을 줄이는 지에 대해서는 밝혀지지 않았다.
미국에서는 현재 POINTER study를 진행하고 있는데, 이는 인지기능이 정상이나 치매의 위험요인이 있는 노인을 대상으로, 운동, 식이조절, 인지훈련, 위험요인관리에 대한 건강상담 등의 multidomain lifestyle intervention을 시행하여 인지기능 향상 및 치매발생 감소의 효과를 보이는 지 보려는 연구로, 이 연구의 sub-study 에서는 MRI와 amyloid, tau PET을 시행하여 intervention을 통해 어떤 imaging biomarker를 가진 사람에서 intervention이 더 효과가 있는지, intervention 이 amyloid pathology 및 cerebrovascular pathology를 감소시키는 지 보려고 계획 중이다 -
결론
이들 내용을 종합해볼 때 가장 중요한 것은 치료에 적합한 대상자를 찾아 적절한 시기에 적합한 치료를 시행하는 것이다.
References
- 1. Jansen WJ, Ossenkoppele R, Knol DL, Tijms BM, Scheltens P, Verhey FR, Visser PJ; Amyloid Biomarker Study Group, Aalten P, Aarsland D, Alcolea D, Alexander M, Almdahl IS, Arnold SE, Baldeiras I, Barthel H, van Berckel BN, Bibeau K, Blennow K, Brooks DJ, van Buchem MA, Camus V, Cavedo E, Chen K, Chetelat G, Cohen AD, Drzezga A, Engelborghs S, Fagan AM, Fladby T, Fleisher AS, van der Flier WM, Ford L, F*rster S, Fortea J, Foskett N, Frederiksen KS, Freund-Levi Y, Frisoni GB, Froelich L, Gabryelewicz T, Gill KD, Gkatzima O, Gómez-Tortosa E, Gordon MF, Grimmer T, Hampel H, Hausner L, Hellwig S, Herukka SK, Hildebrandt H, Ishihara L, Ivanoiu A, Jagust WJ, Johannsen P, Kandimalla R, Kapaki E, Klimkowicz-Mrowiec A, Klunk WE, K*hler S, Koglin N, Kornhuber J, Kramberger MG, Van Laere K, Landau SM, Lee DY, de Leon M, Lisetti V, Lleó A, Madsen K, Maier W, Marcusson J, Mattsson N, de Mendonça A, Meulenbroek O, Meyer PT, Mintun MA, Mok V, Molinuevo JL, Møllerg(rd HM, Morris JC, Mroczko B, Van der Mussele S, Na DL, Newberg A, Nordberg A, Nordlund A, Novak GP, Paraskevas GP, Parnetti L, Perera G, Peters O, Popp J, Prabhakar S, Rabinovici GD, Ramakers IH, Rami L, Resende de Oliveira C, Rinne JO, Rodrigue KM, Rodríguez-Rodríguez E, Roe CM, Rot U, Rowe CC, R+ther E, Sabri O, Sanchez-Juan P, Santana I, Sarazin M, Schr*der J, Sch+tte C, Seo SW, Soetewey F, Soininen H, Spiru L, Struyfs H, Teunissen CE, Tsolaki M, Vandenberghe R, Verbeek MM, Villemagne VL, Vos SJ, van Waalwijk van Doorn LJ, Waldemar G, Wallin A, Wallin "K, Wiltfang J, Wolk DA, Zboch M, Zetterberg H.Jansen WJ, et al. Prevalence of cerebral amyloid pathology in persons without dementia: a meta-analysis. JAMA. 2015 May 19;313(19):1924-38. doi: 10.1001/jama.2015.4668.
- 2. Ossenkoppele R, Jansen WJ, Rabinovici GD, Knol DL, van der Flier WM, van Berckel BN, Scheltens P, Visser PJ; Amyloid PET Study Group, Verfaillie SC, Zwan MD, Adriaanse SM, Lammertsma AA, Barkhof F, Jagust WJ, Miller BL, Rosen HJ, Landau SM, Villemagne VL, Rowe CC, Lee DY, Na DL, Seo SW, Sarazin M, Roe CM, Sabri O, Barthel H, Koglin N, Hodges J, Leyton CE, Vandenberghe R, van Laere K, Drzezga A, Forster S, Grimmer T, Sánchez-Juan P, Carril JM, Mok V, Camus V, Klunk WE, Cohen AD, Meyer PT, Hellwig S, Newberg A, Frederiksen KS, Fleisher AS, Mintun MA, Wolk DA, Nordberg A, Rinne JO, Chételat G, Lleo A, Blesa R, Fortea J, Madsen K, Rodrigue KM, Brooks DJ.Ossenkoppele R, et al. Among authors: jansen wj. Prevalence of amyloid PET positivity in dementia syndromes: a meta-analysis. JAMA. 2015 May 19;313(19):1939-49. doi: 10.1001/jama.2015.4669
- 3. Alifiya Kapasi , Charles DeCarli , Julie A Schneider. Impact of multiple pathologies on the threshold for clinically overt dementia. Acta Neuropathol. 2017 Aug;134(2):171-186. doi: 10.1007/s00401-017-1717-7. Epub 2017 May 9.
- 4. Landau SM, Horng A, Fero A, Jagust WJ; Alzheimer's Disease Neuroimaging Initiative.Landau SM, et al. Amyloid negativity in patients with clinically diagnosed Alzheimer disease and MCI..Neurology. 2016 Apr 12;86(15):1377-1385. doi: 10.1212/WNL.0000000000002576. Epub 2016 Mar 11.
- 5. Liu E, Schmidt ME, Margolin R, Sperling R, Koeppe R, Mason NS, Klunk WE, Mathis CA, Salloway S, Fox NC, Hill DL, Les AS, Collins P, Gregg KM, Di J, Lu Y, Tudor IC, Wyman BT, Booth K, Broome S, Yuen E, Grundman M, Brashear HR; Bapineuzumab 301 and 302 Clinical Trial Investigators.Liu E, et al. Amyloid-β 11C-PiB-PET imaging results from 2 randomized bapineuzumab phase 3 AD trials. Neurology. 2015 Aug 25;85(8):692-700. doi: 10.1212/WNL.0000000000001877. Epub 2015 Jul 24.
- 6. Boyle PA, Yu L, Wilson RS, Leurgans SE, Schneider JA, Bennett DA.Boyle PA, et al. Person-specific contribution of neuropathologies to cognitive loss in old age. Ann Neurol. 2018 Jan;83(1):74-83. doi: 10.1002/ana.25123.
- 7. Boyle PA, Yu L, Leurgans SE, Wilson RS, Brookmeyer R, Schneider JA, Bennett DA.Boyle PA, et al. Attributable risk of Alzheimer's dementia attributed to age-related neuropathologies. Ann Neurol. 2019 Jan;85(1):114-124. doi: 10.1002/ana.25380.
- 8. Nelson PT, Dickson DW, Trojanowski JQ, Jack CR, Boyle PA, Arfanakis K, Rademakers R, Alafuzoff I, Attems J, Brayne C, Coyle-Gilchrist ITS, Chui HC, Fardo DW, Flanagan ME, Halliday G, Hokkanen SRK, Hunter S, Jicha GA, Katsumata Y, Kawas CH, Keene CD, Kovacs GG, Kukull WA, Levey AI, Makkinejad N, Montine TJ, Murayama S, Murray ME, Nag S, Rissman RA, Seeley WW, Sperling RA, White Iii CL, Yu L, Schneider JA.Nelson PT, et al. Limbic-predominant age-related TDP-43 encephalopathy (LATE): consensus working group report. Brain. 2019 Jun 1;142(6):1503-1527. doi: 10.1093/brain/awz099
- 9. Shama Karanth , Peter T Nelson , Yuriko Katsumata , Richard J Kryscio , Frederick A Schmitt , David W Fardo, Matthew D Cykowski, Gregory A Jicha , Linda J Van Eldik, Erin L Abner. Prevalence and Clinical Phenotype of Quadruple Misfolded Proteins in Older Adults. JAMA Neurol. 2020 Jun 22;e201741. doi: 10.1001/jamaneurol.2020.1741.
- 10. Jack CR Jr, Knopman DS, Jagust WJ, Petersen RC, Weiner MW, Aisen PS, Shaw LM, Vemuri P, Wiste HJ, Weigand SD, Lesnick TG, Pankratz VS, Donohue MC, Trojanowski JQ.Jack CR Jr, et al. Tracking pathophysiological processes in Alzheimer's disease: an updated hypothetical model of dynamic biomarkers. Lancet Neurol. 2013 Feb;12(2):207-16. doi: 10.1016/S1474-4422(12)70291-0.
- 11. Victor L Villemagne, Samantha Burnham, Pierrick Bourgeat, Belinda Brown, Kathryn A Ellis, Olivier Salvado, Cassandra Szoeke, S Lance Macaulay, Ralph Martins, Paul Maruff, David Ames, Christopher C Rowe, Colin L Masters, Australian Imaging Biomarkers and Lifestyle (AIBL) Research Group. Amyloid β deposition, neurodegeneration, and cognitive decline in sporadic Alzheimer's disease: a prospective cohort study. Lancet Neurol. 2013 Apr;12(4):357-67. doi: 10.1016/S1474-4422(13)70044-9
- 12. Stephanie L Leal, Susan M Landau, Rachel K Bell , William J Jagust. Hippocampal activation is associated with longitudinal amyloid accumulation and cognitive decline. Elife. 2017 Feb 8;6:e22978. doi: 10.7554/eLife.22978
- 13. Gottesman RF, Albert MS, Alonso A, Coker LH, Coresh J, Davis SM, Deal JA, McKhann GM, Mosley TH, Sharrett AR, Schneider ALC, Windham BG, Wruck LM, Knopman DS.Gottesman RF, et al. Associations Between Midlife Vascular Risk Factors and 25-Year Incident Dementia in the Atherosclerosis Risk in Communities (ARIC) Cohort. JAMA Neurol. 2017 Oct 1;74(10):1246-1254. doi: 10.1001/jamaneurol.2017.1658.
- 14. Ruth Peters, Andrew Booth, Kenneth Rockwood, Jean Peters, Catherine D'Este, Kaarin J Anstey. Combining modifiable risk factors and risk of dementia: a systematic review and meta-analysis. BMJ Open 2019;9:e022846. doi:10.1136/bmjopen-2018-022846
- 15. Kim HJ, Park S, Cho H, Jang YK, San Lee J, Jang H, Kim Y, Kim KW, Ryu YH, Choi JY, Moon SH, Weiner MW, Jagust WJ, Rabinovici GD, DeCarli C, Lyoo CH, Na DL, Seo SW.Kim HJ, et al. Among authors: kim y, kim kw. Assessment of Extent and Role of Tau in Subcortical Vascular Cognitive Impairment Using 18F-AV1451 Positron Emission Tomography Imaging. JAMA Neurol. 2018 Aug 1;75(8):999-1007. doi: 10.1001/jamaneurol.2018.0975.
- 16. Christopher A. Lane, Josephine Barnes, Jennifer M. Nicholas, Carole H. Sudre, David M. Cash, Ian B. Malone, Thomas D. Parker, Ashvini Keshavan, Sarah M. Buchanan, Sarah E. Keuss, Sarah-Naomi James, Kirsty Lu, Heidi Murray-Smith, Andrew Wong, Elizabeth Gordon, William Coath, Marc Modat, David Thomas, Marcus Richards, Nick C. Fox, Jonathan M. Schott. Associations Between Vascular Risk Across Adulthood and Brain Pathology in Late Life Evidence From a British Birth Cohort. JAMA Neurol. 2020;77(2):175-183. doi:10.1001/jamaneurol.2019.3774
- 17. Jennifer S. Rabin, Hyun-Sik Yang, Aaron P. Schultz, Bernard J. Hanseeuw, Trey Hedden, Anand Viswanathan, Jennifer R. Gatchel, Gad A. Marshall, Emily Kilpatrick, Hannah Klein, Vaishnavi Rao, Rachel F. Buckley, Wai-Ying Wendy Yau, Dylan R. Kirn, Dorene M. Rentz, Keith A. Johnson, MD,2,3,4,8 Reisa A. Sperling, and Jasmeer P. Chhatwal. Vascular risk and β-amyloid are synergistically associated with cortical tau. Ann Neurol. 2019 Feb; 85(2): 272–279. doi: 10.1002/ana.25399
- 18. Bruce Reed , Sylvia Villeneuve , Wendy Mack, Charles DeCarli , Helena C Chui, William Jagust. Associations between serum cholesterol levels and cerebral amyloidosis. JAMA Neurol. 2014 Feb;71(2):195-200. doi: 10.1001/jamaneurol.2013.5390.
- 19. Tiia Ngandu , Jenni Lehtisalo , Alina Solomon , Esko Lev'lahti, Satu Ahtiluoto , Riitta Antikainen, Lars B'ckman, Tuomo H'nninen, Antti Jula, Tiina Laatikainen, Jaana Lindstr*m, Francesca Mangialasche, Teemu Paajanen, Satu Pajala, Markku Peltonen , Rainer Rauramaa, Anna Stigsdotter-Neely, Timo Strandberg, Jaakko Tuomilehto, Hilkka Soininen, Miia Kivipelto. A 2 year multidomain intervention of diet, exercise, cognitive training, and vascular risk monitoring versus control to prevent cognitive decline in at-risk elderly people (FINGER): a randomised controlled trial. Lancet. 2015 Jun 6;385(9984):2255-63. doi: 10.1016/S0140-6736(15)60461-5.
- 20. SPRINT MIND Investigators for the SPRINT Research Group, Williamson JD, Pajewski NM, Auchus AP, Bryan RN, Chelune G, Cheung AK, Cleveland ML, Coker LH, Crowe MG, Cushman WC, Cutler JA, Davatzikos C, Desiderio L, Erus G, Fine LJ, Gaussoin SA, Harris D, Hsieh MK, Johnson KC, Kimmel PL, Tamura MK, Launer LJ, Lerner AJ, Lewis CE, Martindale-Adams J, Moy CS, Nasrallah IM, Nichols LO, Oparil S, Ogrocki PK, Rahman M, Rapp SR, Reboussin DM, Rocco MV, Sachs BC, Sink KM, Still CH, Supiano MA, Snyder JK, Wadley VG, Walker J, Weiner DE, Whelton PK, Wilson VM, Woolard N, Wright JT Jr, Wright CB.SPRINT MIND Investigators for the SPRINT Research Group, et al. Effect of Intensive vs Standard Blood Pressure Control on Probable Dementia: A Randomized Clinical Trial. JAMA. 2019 Feb 12;321(6):553-561. doi: 10.1001/jama.2018.21442.
Biomarker of vascular cognitive impairment and dementia; informing disease mechanism
명지병원 정영희
Donna M Wilcock PhD, University of Kentucky
치매환자들을 뇌부검을 해보면 임상적으로 알츠하이머 진단받은 환자들도, small vessel disease, TDP 43에 의한 LATE 등 다양한 pathology 가 존재한다. 최근 알츠하이머 병 뿐만 아니라 VCID 에 대한 fluid biomarker 도 개발되고 있다. 미국에서 MarkVICID 라는 consortium을 만들어서small vessel disease biomarker를 개발하고 cross site validation 을 하고 있다.
-
Endothelial signaling kit (VEGF-D, PlGF, bFGF)
- 초기 뇌혈관질환에서의 endothelial dysfunction 이 보상적으로 endothelial, angiogenesis signaling을 upregulation 시킴.
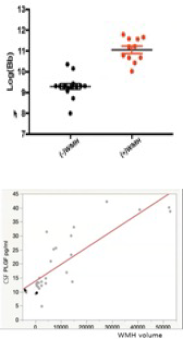
- longitudinal preliminary data에 따르면 baseline signal 이 가속화된 백질 손상과 인지저하를 예측할 수 있음.
- cross-sectional data에서 (아밀로이드 PET 에서의 amyloid를 보정하였을 때도) endothelial signaling이 증가하면 cerebral free water 가 증가되고 전체 뇌의 FA 값이 감소함.
References : 제시된 결과들이 주로 예비연구 결과로 publish 된 논문을 찾기 어려웠습니다
Neuroimaging: Imaging The Human Synapse In AD
전북대병원 김고운
Session Chairs: Joana Pereira, Eric Salmon.
UCB J PET은 synaptic vesicle glycoprotein 2A 에 붙는 tracer 를 이용한 PET 입니다. 2014년에 처음
개발이 되었고, presynapse 의 SV2A 에 붙어서 Synaptic vesicle 의 density 를 측정하게 됩니다. CSF biomarker로는 Neurogranin, Gap-43, SNAP-25, SYT1 이 있는데, Neurogranin은 postsynaptic, Gap-43, SNAP-25, SYT1 는 presynaptic protein을 반영하는 biomarker입니다.
1) Ayla Mansur et al. Characterization of 3 PET Tracers for Quantification of Mitochondrial and Synaptic Function in Healthy Human Brain: 18F-BCPP-EF, 11C-SA-4503, and 11C-UCB-J J Nucl Med 2020 61:96-103
-
Association between Cerebral Amyloid Accumulation and Synaptic Density in Alzheimer’s Disease: A Multitracer PET Study, Ryan S. O'Dell.
Amyloid pathology 와 synaptic density의 correlation을 보았던 연구인데, UCB J PET과 Pib PET data 를 분석하였고, AMCI에서는 hippocampal synaptic density 와 pib global amyloid deposition이 negative correlation을 보이는 반면, AD에서는 cortical synaptic density 가 와 Pib PET global amyloid deposition이 negative correlation을 보였습니다.
1) Chen MK et al. Assessing Synaptic Density in Alzheimer Disease With Synaptic Vesicle Glycoprotein 2A Positron Emission Tomographic Imaging. JAMA Neurol. 2018 Oct 1;75(10):1215-1224 -
Regional tau pathology is associated with loss of synapses and reduced synaptic activity: a combined [18F]flortaucipir, [11C]UCB-J and magnetoencephalography study, Emma M. Coomans.
Tau pathology 와 synaptic density 그리고 synaptic activity 의 연관성을 보여준 연구입니다. Tau PET, UCB J PET, MEG data를 분석하였고, Tau PET에서 uptake가 증가하는 영역에서 UCB J PET 은 reciprocal하게 uptake가 떨어지는 것을 볼 수 있습니다. 또한 MEG 에서는 Tau uptake 가 증가하는 경우 delta activity가 더 증가하여서, Tau pathology는 synaptic loss 그리고 oscillatory slowing과 관련이 있음을 보여주었습니다.
1) Ehrenberg AJ, Khatun A, Coomans E, et al. Relevance of biomarkers across different neurodegenerative diseases [published correction appears in Alzheimers Res Ther. 2020 Jun 9;12(1):71 -
Microglial activation indexed by [11C]PBR28 is associated with synaptic depletion in theAlzheimer’s disease spectrum., Joseph Therriault.
Neuroinfammation biomarker와 CSF synaptic biomarker의 연관성을 보여준 연구입니다. Microglial activation을 보여주는 TSPO PET 과 CSF synaptic biomarker 그리고 CSF inflammation biomarker를 분석하였습니다. SNAP-25 가 TSPO PET과 가장 좋은 correlation을 보여주었고 CSF에서는 SNAP-25, SYT1이 TREM2, YKL40와 가장 correlation을 보여주었습니다. 따라서 synaptic biomarker는 neuroinflammation biomarker와 관련이 있음을 알 수 있습니다.
-
Untangling the roles of amyloid and tau in synaptic and axonal loss in the course of Alzheimer’s disease, Joana B. Pereira.
초기단계에서는 Ng 의 증가가 amyloid PET, fMRI와 와 positive correlation을 보여주었고 후기단계에서는 NfL 증가가 tau PET 와 positive correlation, Tau PET은 DTI에서 Parahippocampal tract의 FA값과 negative correlation을 보여주어서, 연구자의 가설인 Amyloid deposition이 먼저 발생하고, synaptic change가 진행하고, 이어서 Tau deposition이 있고 axonal degeneration 순서로 진행한다는 것을 뒷받침 해주었습니다.
-
SNAP25 reflects amyloid- and tau-related synaptic damage: associations between PET, VBM and cerebrospinal fluid biomarkers of synaptic disfunction in the Alzheimer’s disease spec trum, Andréa Lessa Benedet.
Amyloid PET, tau PET, sMRI, CSF biomarker를 분석하였고 SNAP-25가 모든 image과 가장 좋은 correlation을 보였습니다.